El problema clínico
Los accidentes cerebrovasculares (ACV) isquémicos criptogénicos (ACV-IC) son infartos cerebrales sintomáticos cuya causa probable no se identifica después de una evaluación diagnóstica adecuada. El uso de de definiciones más amplias permite el diagnóstico de más ACV en los pacientes que fueron evaluados en forma incompleta y en aquellos con más de una causa probable identificada, pero el autor piensa que es mejor que estos casos sean considerados como entidades separadas.
Entre los ACV de causa indeterminada es útil establecer más diferencias entre los ACV que son criptogénicos después de la evaluación estándar y los que son criptogénicos después de una evaluación especializada y, entre los que son "altamente criptogénicos" (es decir, sin ninguna causa posible o probable descubierta) y los "de origen posiblemente determinado" (es decir, sin causa probable pero con una o más causas posibles identificadas).
Los mecanismos criptogénicos representan el 10% al 40% de todos los ACV isquémicos. Este rango es producto de las diferentes definiciones utilizadas a través de la serie, la evolución de la tecnología diagnóstica, las diferentes concepciones de la investigación etiológica adecuada y el hecho de que hay más de 200 causas conocidas de ACV isquémico que sería necesario excluir.
En general, el porcentaje de ACV isquémicos que se clasifican como criptogénicos ha disminuido con el tiempo a medida que se han ido perfeccionando las pruebas de diagnóstico, pasando del 40% en la década de 1970 al 10-15% en la actualidad, en los centros altamente especializados. Sin embargo, el ACV-IC después de una evaluación diagnóstica estándar sigue siendo un problema clínico frecuente, representando el 20-30% de todos los ACV isquémicos.
Las causas determinantes más comunes del ACV isquémico que se identifican durante la evaluación rutinaria inicial son la aterosclerosis y el cardioembolismo de las grandes arterias y, la enfermedad de los vasos pequeños, cada una de las cuales es responsable de aproximadamente el 25% de los casos.
A menudo, en los pacientes con diagnóstico presuntivo de ACV-IC después de la evaluación estándar, la realización de estudios más especializados permite arribar al diagnóstico etiológico, como la aterosclerosis oculta, incluyendo las placas no estenosantes pero inestables en zonas intracraneanas y sitios cervicales o las placas estenosantes en el tórax y del origen de la carótida común y las arterias vertebrales torácicas; las arteriopatías no ateroscleróticas como la disección o la vasculitis; los estados de hipercoagulabilidad; el cardioembolismo de grado medio como la fibrilación auricular paroxística de baja carga o la miocardiopatía dilatada de grado moderado y, la embolia paradójica.
La edad del paciente influye en la probabilidad de las diversas causas. En los adultos jóvenes de 18 a 30 años es más común la disección pero la trombofilia congénita y la enfermedad cardíaca también son causas destacables. En las personas de 31 a 60 años, la aterosclerosis precoz y la enfermedad cardíaca estructural con baja carga son cada vez más comunes. En los pacientes >60 años es más frecuente la fibrilación auricular oculta.
En comparación con los ACV de origen determinado, generalmente los ACV criptogénicos provocan déficits neurológicos y discapacidad final de menor gravedad y una mortalidad más baja. En la mayoría pero no en todos los estudios de seguimiento a largo plazo, los pacientes con ACV-IC tienen menor riesgo de recurrencia que aquellos con ACV de causa identificada.
En el estudio a largo plazo más grande realizado hasta la fecha, los pacientes de 18 a 55 años que sufrieron un ACV-IC y fueron tratados con aspirina mostraron una tasa de recurrencia del 1,9% en el primer año después del ACV, y del 0,8%/año a los 2 a 4 años. Esta tasa baja de recurrencia concuerda con la ausencia de una causa fácilmente identificable de ACV mayor que colocaría al paciente en un riesgo elevado.
| Puntos clínicos clave ACV criptogénico • En la cuarta parte de los pacientes con ACV isquémico no se halla ninguna causa probable después de la evaluación estándar, incluyendo la ecocardiografía, la telemetría cardiaca o el Holter de 24 horas en los pacientes hospitalizados, las imágenes por RM o TC para ver las características topográficas del infarto cerebral y, la TC angiográfica de las arterias del cuello y el cerebro. La investigación adicional identifica el mecanismo probable en más de la mitad de estos pacientes. • La mayoría de los ACV-IC se produce por émbolos que se originan en las arterias proximales, el corazón o las venas (si hay cortocircuito de derecha a izquierda). • El estudio de los pacientes con ACV-IC incluye la evaluación de las arteriopatías ateroscleróticas y no ateroscleróticas, el origen cardíaco de de las embolias (anormalidades estructurales y arritmias) y, los trastornos de la coagulación. • El foramen oval permeable se encuentra hasta en la mitad de los adultos jóvenes con ACV-IC, pero también se halla en la cuarta parte de las personas sanas. • La fibrilación auricular paroxística oculta de baja carga se reconoce cada vez más como causa de ACV criptogénico, especialmente en los pacientes de edad avanzada |
Estrategias y evidencia
Evaluación del paciente con accidente cerebrovascular isquémico criptogénico
El ACV-IC es un diagnóstico de exclusión al que se arriba descartando las causas conocidas. En la práctica actual, la evaluación de rutina del paciente con ACV isquémico tiene varios componentes. Las características topográficas del ACV (localización y volumen del infarto y su multiplicidad) se evalúan mediante la RM cerebral, incluyendo las secuencias de difusión (que son más sensibles para las lesiones pequeñas y del tronco cerebral y cerebelo) o la tomografía computarizada (TC) del cerebro (si no se dispone de la RM).
Las características topográficas proporcionan importantes pistas etiológicas: la presencia de infartos en varios territorios sugiere émbolos de un origen aortocardíaco proximal; los infartos de diferente antigüedad en un solo territorio sugieren émbolos de origen arterial; los infartos a lo largo de los límites del territorio de la arteria cerebral hacen sospechar una hipotensión sistémica o la embolia múltiple y, un infarto pequeño y profundo junto con imágenes hiperintensas en la sustancia blanca sugiere una enfermedad intrínseca de los pequeños vasos. Las arterias del cerebro, el cuello y el tórax se evalúan por angiografía por RM o TC (cuyas sensibilidad y especificidad son similares) o, si éstas están contraindicadas o no están disponibles se puede recurrir a la ecografía dúplex carotídea y a la ecografía Doppler transcraneana.
La presencia de una enfermedad cardíaca estructural se evalúa mediante la ecocardiografía. El ecocardiograma transtorácico (ETT) permite visualizar mejor el ventrículo y se utiliza para el estudio de los pacientes con enfermedad arterial coronaria, insuficiencia cardíaca u otra enfermedad ventricular detectada por la historia o el electrocardiograma (ECG).
En los pacientes con infarto no lacunar sin evidencia de enfermedad ventricular, la ecocardiografía transesofágica (ETE) permite ver bien la aurícula y el arco aórtico se prefiere como estudio adicional en los pacientes con resultados poco reveladores en la ETT. La ETE identifica a las anomalías potencialmente más destacadas en aproximadamente el 50-75% de los pacientes jóvenes con ACV-IC, incluyendo el foramen oval permeable, el aneurisma del septo interauricular, la endocarditis, la aterosclerosis aórtica, la disfunción de la pared miocárdica regional, la dilatación de la aurícula izquierda y los trombos de la orejuela auricular.
Las arritmias cardíacas son evaluadas inicialmente mediante el ECG de 12 derivaciones y la telemetría cardiaca o el monitoreo Holter de 24 horas se utilizan para los pacientes hospitalizados. Los trastornos hematológicos se estudian mediante el hemograma, el tiempo de protrombina y el tiempo de parcial de tromboplastina
| Hallazgos sugestivos en la historia y la semiología de los pacientes con ACV-IC | |
| Variable | Consecuencias clínicas potenciales |
| Características de la historia | |
| Trauma o manipulación del cuello | Disección de la carótida o de la arteria vertebral |
| Migraña | Infarto migrañoso o CADASIL* |
| Uso de drogas intravenosas | Endocarditis, infección por VIH, vasculitis, embolia paradójica o vasoespasmo |
| Procedimiento dental o infección bacteriana sistémica | Endocarditis, embolia séptica o coagulopatía |
| Viaje en avión o maniobra de Valsalva al comienzo del ACV | Embolismo paradójico |
| Historia familiar de infarto de miocardio precoz o de ACV isquémico | Arteriosclerosis genética acelerada |
| Embarazo o periparto | Trombosis venosa cerebral o eclampsia |
| Anemia de células falciformes | Enfermedad moyamoya secundaria |
| Signos físicos | |
| Presión arterial asimétrica en los brazos | Coartación de aorta, disección aórtica, enfermedad de Takayasu o aterosclerosis prematura |
| Piel Marcas de pinchazos Livedo reticularis Xantoma o xantelasma | Uso de drogas intravenosas, infección por VIH Síndrome de Sneddon, síndrome de anticuerpos antifosfolípidos o lupus eritematoso sistémico HIperlipidemia |
| Adenopatía | Infección, sarcoidosis o enfermedad de Tangier |
| Soplo cardíaco | Endocarditis, defecto septal o mixoma |
| Vasos Pulsos disminuídos Soplo Trombosis venos de las piernas | Aterosclerosis prematura, coartación aórtica, disección aórtica o enfermedad de Takayasu Aterosclerosis precoz, displasia fibromuscular o disección aterosclerosis precoz, displasia arterial Estado de hipercoagulabilidad |
| *CADASIL: denota la arteriopatía cerebral autosómica dominante con infartos subcorticales y leucoencefalopatía, y el virus de la inmunodeficiencia humana VIH | |
| El ACV puede ser considerado como criptogénico cuando la evaluación clínica estándar y las imágenes cerebrales sugieren un infarto grande, profundo o superficial, pero sin hallazgos en las imágenes cardiacas o con análisis hematológicos que no revelan una causa probable. |
Los pacientes con un infarto profundo y pequeño también pueden ser considerados portadores de un ACV-IC si son menores de 50 años, no tienen ningún factor de riesgo vascular estándar, ni hiperintensidades en la sustancia blanca, o si previamente no han sufrido infartos pequeños y profundos. Seguidamente, se harán estudios diagnósticos más especializados.
Para clasificar los ACV isquémicos en los ACV que tienen una causa conocida o los ACV que son criptogénicos se han desarrollado varios algoritmos de diagnósticos. El Trial of Org 10172 en el algoritmo diagnóstico Acute Stroke Treatment (TOAST) está siendo superado por el ASCOD (Atherosclerosis, Small-vessel disease, Cardiac, Other, Dissection: aterosclerosis, enfermedad de los vasos pequeños, cardiaco, otros, disección), más nuevo, y el sistema Causative Clasification of Stroke (CCS) que tienen un enfoque más graduado cuando son varias las causas que se identifican.
En comparación con el TOAST, tanto el ASCOD como los sistemas CCS identifican a un menor número de pacientes con diagnóstico de ACV-IC. Estos instrumentos son esenciales para la clasificación de los pacientes en los ensayos clínicos y pueden ser útiles en la práctica clínica.
Esta revisión solo está enfocada en las causas de ACV-IC que actualmente despiertan mayor interés como la fibrilación auricular oculta, el foramen oval permeable y la embolia cerebral de origen indeterminado.
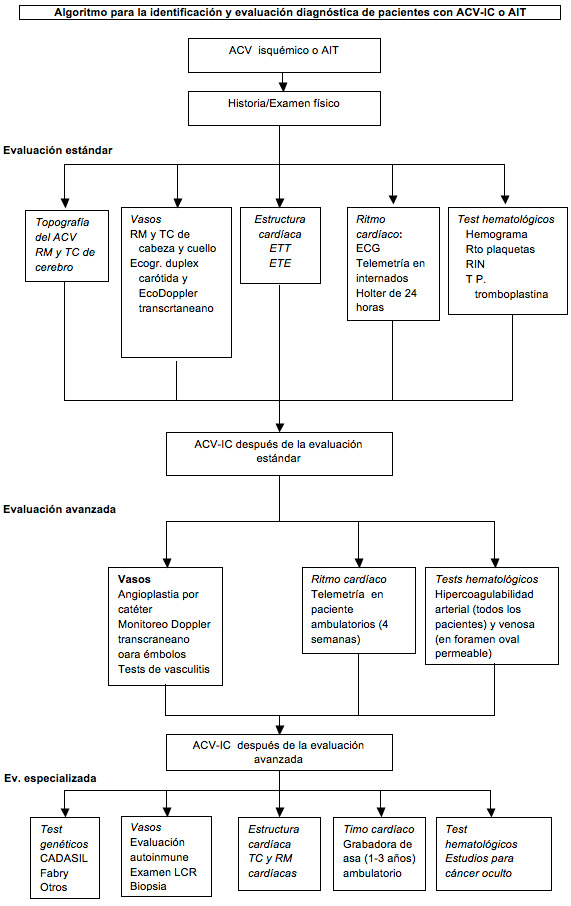
Algoritmo para la identificación y evaluación diagnóstica de pacientes con ACV-IC o AIT
|
Fibrilación auricular oculta
La fibrilación auricular manifiesta es una causa común del ACV isquémico, el que representa a la cuarta parte de todos los infartos cerebrales y a más de la mitad de los infartos de origen cardioembólico. En la evaluación estándar del ACV isquémico, casi el 15% de los pacientes tiene una historia conocida de fibrilación auricular crónica o paroxística previa al ACV; casi el 8% recibe el diagnóstico de fibrilación auricular de reciente comienzo por los hallazgos del primer ECG y otro 5% recibe el diagnóstico de fibrilación auricular de reciente comienzo después de la presentación inicial con ritmo sinusal por los resultados de la telemetría cardiaca o el monitoreo Holter de 24 horas realizados en los pacientes hospitalizados,
La tecnología para detectar la fibrilación auricular paroxística infrecuente ha mejorado notablemente en los últimos 10 años debido al desarrollo de los sistemas de telemetría cardíaca móvil que pueden ser usados externamente durante 2 a 4 semanas, los grabadores de asa subcutáneos que tienen una batería de larga duración que permite detectar la fibrilación durante 1 a 3 años y, en los pacientes que necesitan marcapasos internos terapéuticos o desfibriladores, dispositivos terapéuticos implantables con capacidad para detectar la fibrilación auricular durante ≥3 años.
Estos avances tecnológicos pusieron de manifiesto a un grupo de pacientes con fibrilación auricular paroxística de baja carga muy sospechados pero pocas veces identificados. Los pacientes con fibrilación auricular paroxística de baja carga tienen menor riesgo de ACV que los pacientes con fibrilación auricular crónica o paroxística de alta carga. Sin embargo, el riesgo de ACV es mayor que entre las personas sin fibrilación auricular. La ocurrencia de tan solo un episodio de una hora de fibrilación auricular en 2 años de seguimiento se ha asociado a una duplicación del riesgo de ACV. Isquémico.
En el 15% de los pacientes cuyos ACV isquémicos se consideran criptogénicos después de la evaluación convencional realizada durante su hospitalización, el monitoreo cardíaco ambulatorio prolongado detecta la fibrilación auricular de baja carga. En el estudio multicéntrico Cryptogenic Stroke and Underlying AF (CRYSTAL AF), la frecuencia de la detección de la fibrilación auricular paroxística fue del 9% a los 6 meses; 12% al año y 30% a los 3 años.
Las características de los pacientes que tienen mayor probabilidad de que la vigilancia prolongada descubra la fibrilación auricular de baja carga son la edad avanzada y el puntaje más elevado del CHA2DS2-VASc (en el que los puntajes van del 0 al 9; los puntajes más elevados indican mayor riesgo), las características topográficas del infarto cerebral (tales como la afectación de varios territorios vasculares y la ubicación cortical) y los índices de cardiopatía auricular izquierda, incluyendo la dilatación de la aurícula izquierda, la deformación y la reducción de la fracción de vaciado, el tamaño de la orejuela auricular izquierda, la dispersión de la onda P en el ECG, las extrasístoles auriculares frecuentes y los niveles del N-terminal pro-péptido natriurético cerebral elevado en el suero.
Actualmente se desconoce si los pacientes con fibrilación auricular de baja carga se tratan mejor con anticoagulantes o con agentes antiplaquetarios. En algunos, es probable que la fibrilación auricular infrecuente no sea una causa relacionada con el ACV; hay pocos ensayos clínicos que ayuden a tomar decisiones. Un ensayo aleatorizado reciente de personas con desfibriladores implantados no mostró una reducción significativa de un resultado compuesto por ACV, embolia sistémica y hemorragia grave, utilizando la detección de la fibrilación o el aleteo auricular oculto para guiar la indicación de warfarina, en comparación con la atención clínica de rutina.
Sin embargo, algunos pacientes tenían antecedentes de isquemia cerebral, muchos del grupo de control recibieron anticoagulantes y la warfarina fue suspendida en el grupo de seguimiento después de períodos de 1 a 3 meses sin fibrilación auricular. A la espera de la finalización de ensayos en curso se ha sugerido un algoritmo provisorio.
Foramen oval permeable
El embolismo paradójico es el pasaje de un coágulo u otra partícula embólica de la circulación venosa a la circulación arterial, a través de un cortocircuito de derecha a izquierda, como sucede en el defecto del tabique auricular o ventricular y en la malformación arteriovenosa pulmonar. La causa más común de este defecto es el foramen oval permeable. Esta comunicación interauricular se cierra normalmente dentro de los 3 meses posteriores al nacimiento, pero puede persistir durante toda la vida y potencialmente permite la tromboembolia venosa evitando el pasaje de los émbolos a los vasos pulmonares y su introducción en la circulación arterial sistémica.
El diámetro medio de un foramen oval permeable es de 4,9 mm, que es más que suficiente para permitir el paso de émbolos que son lo suficientemente grandes como para ocluir el tronco de la arteria cerebral media (3 mm) y las ramas corticales principales (1 mm). El aneurisma del septo auricular─un tabique interauricular hipermóvil que sobresale alternativamente en ambas aurículas─es una anormalidad relacionada que ha sido asociada a un riesgo mayor de ACV en los pacientes con un foramen oval permeable.
El foramen oval permeable está presente en aproximadamente la cuarta parte de la población general pero en la mitad de los pacientes con ACV-IC. Un análisis del riesgo atribuible Bayesiano de los datos agrupados de 12 estudios sugiere que en los pacientes con ACV-IC que tenían un foramen oval permeable, dicha cardiopatía probablemente esté relacionada causalmente con el ACV en casi la mitad de los casos.
Las características que aumentan la probabilidad de una relación causal son la edad más joven; la maniobra de Valsalva al comienzo del ACV; el viaje prolongado en avión o en automóvil antes del ACV; la trombosis venosa concomitante en la pierna o la pelvis; el estado de hipercoagulabilidad venosa concomitante; la coexistencia de un aneurisma del septo auricular; el antecedente de migraña con aura; la ubicación cortical, la multiplicidad y gran tamaño de los infartos cerebrales y, la ausencia de hipertensión, diabetes y tabaquismo.
El diagnóstico de foramen oval permeable se basa en la ecografía con sustancia de contraste salino agitada ("burbuja"). La ETT detecta aproximadamente solo la mitad de los casos de foramen oval permeable hallados en la ETE o la ecografía Doppler transcraneana. La ecografía Doppler no brinda información simultánea sobre otras lesiones cardiacas estructurales y la aterosclerosis del arco aórtico. En consecuencia, el método preferencial es la ETE.
Cuando existen contraindicaciones para la ETE y la ETT si es poco reveladora, se utiliza la ecogrrafía Doppler transcraneana con material de contraste en burbujas. En los pacientes con un foramen oval permeable, la evidencia de que puede estar relacionado causalmente con el ACV puede obtenerse mediante otros estudios como el estado de hipercoagulabilidad venosa y la detección de trombos venosos profundos ocultos, utilizando la ecografía de las piernas y la RM o la TC de la pelvis.
Una opción terapéutica de primera línea para los pacientes con ACV-IC que tienen un foramen oval permeable es el uso de antiplaquetarios; la administración de 300 mg/día de aspirina en estos pacientes se asocia con tasas bajas de ACV recurrente. El metaanálisis de datos de observación y ensayos aleatorizados muestra que la warfarina tiene una eficacia similar o mayor que la aspirina, especialmente en los pacientes con infartos en territorios superficiales. Los anticoagulantes directos orales más nuevos no han sido probados formalmente en los pacientes con foramen oval permeable, pero su eficacia para la prevención y el tratamiento del tromboembolismo venoso sugiere un posible beneficio en la embolia paradójica.
La colocación endovascular percutánea de dispositivos de cierre puede corregir el foramen oval permeable. Las complicaciones, aunque menos frecuentes con los nuevos dispositivos de disco que con los más antiguos con cierre paraguas, incluyen la fibrilación auricular (en casi el 0,7% pacientes/año) y la embolización del dispositivo durante la intervención; el taponamiento cardíaco y el hematoma femoral (cada uno ocurre en <0,5% de los participantes de los ensayos clínicos).
Tres ensayos aleatorizados (uno utilizó un dispositivo de cierre paraguas y los otros dos utilizaron un dispositivo de cierre disco) no mostraron tasas significativamente menores de ACV isquémico recurrente con el tratamiento con dispositivo comparado con el tratamiento médico solo. Sin embargo, un análisis posterior de datos agrupados de pacientes individuales mostró una reducción significativa del riesgo de ACV isquémico recurrente con el dispositivo de cierre disco, de casi 6 a aproximadamente 2 ACV cada 100 pacientes tratados durante un período de 5 años.
Accidente cerebrovascular embólico de origen indeterminado
Los ACV-IC superficiales o profundos pero grandes casi siempre se deben a émbolos que llegan al cerebro originados en una arteria, el corazón o transcardíacos. Entre las causas poco comunes se hallan las enfermedades intrínsecas de las grandes arterias como la trombosis in situ o el vasoespasmo. Recientemente, este concepto clínico largamente establecido fue redefinido como "ACV embólico de origen indeterminado." Estos ACV embólicos de origen indeterminado son operacionalmente definidos como infartos cerebrales no lacunares sin estenosis arterial proximal importante ni origen cardioembólico mayor y representan el 80-90% de todos ACV-IC.
Los infartos hallados en los ACV embólicos de origen indeterminado provienen de diversos orígenes de bajo riesgo como la disfunción ventricular izquierda leve, la calcificación del anillo mitral, la fibrilación auricular paroxística de baja carga, el foramen oval permeable, la aterosclerosis del arco aórtico y las placas ateroscleróticas no estenosantes en las arterias cervicales e intracraneanas.
El beneficio relativo de la anticoagulación versus el tratamiento antiplaquetario no ha sido bien establecido para cualquiera de estas entidades. Se están haciendo grandes ensayos internacionales para comparar los anticoagulantes orales directos nuevos con la aspirina en los pacientes con un ACV de origen indeterminado. A la espera de su finalización es razonable iniciar el tratamiento ya sea con agentes antiplaquetarios o con anticoagulantes orales directos, mientras se continúan los estudios más detallados para hallar su etiología.
Áreas de incertidumbre
A menudo, en los pacientes con ACV-IC se hacen estudios más especializados y costosos que dejan poco rendimiento. Aun no se ha estudiado bien cuál es el enfoque más rentable para su evaluación y cuál es la utilidad de los estudios muy especializados. Se desconoce cuál es la duración más eficaz del monitoreo ambulatorio de la fibrilación auricular de baja carga. La continuación de los estudios para hallar la etiología no debe retrasar el inicio de un plan de tratamiento razonable.
Los estudios adicionales son necesarios para ayudar a los médicos a discriminar si la fibrilación auricular paroxística de baja carga tiene una relación probable con el ACV o es meramente incidental. Para estimar la probabilidad de que el foramen oval permeable sea la causa del ACV-IC se ha desarrollado un puntaje de riesgo pero su potencial para guiar la terapia requiere datos de estudios adicionales. Se necesitan datos de ensayos clínicos rigurosos que comparen los resultados del tratamiento antiplaquetario con el anticoagulante en los pacientes con ACV embólico de origen indeterminado y en los pacientes con fibrilación auricular oculta. También se requieren datos de otros ensayos que comparen los antiplaquetarios, los anticoagulantes y los tratamientos con dispositivos en los pacientes cuyo ACV-IC haya sido atribuido al foramen oval permeable.
Guías
La American Heart Association–American Stroke Association y la American Academy of Neurology–ha publicado guías para el diagnóstico del ACV isquémico y el tratamiento del ACV-IC.
Conclusiones y recomendaciones
El paciente del caso aquí presentado presenta un ACV atribuible a un émbolo que ocluyó brevemente la arteria basilar y luego se trasladó hasta ocluir en forma persistente una rama de la arteria cerebral posterior derecha. Este caso de un ACV embólico de origen aún no determinado permite hacer consideraciones etiológicas que incluyen la aterosclerosis del arco aórtico, el foramen oval permeable con aneurisma del septo auricular, la fibrilación auricular oculta y los estados protrombóticos.
El autor propone proseguir los estudios del paciente con un ETE, los análisis de laboratorio para la hipercoagulabilidad arterial y, debido a un posible cortocircuito de derecha a izquierda en la ETT, agregar el análisis de laboratorio para evaluar la hipercoagulabilidad venosa junto con un plan de monitoreo cardíaco ambulatorio de 4 semanas. Su hipertensión debe ser controlada, y para el tratamiento antitrombótico, el autor propone la aspirina, a la espera de los resultados de los exámenes adicionales para así elegir el tratamiento antiplaquetario o anticoagulante a largo plazo adecuado.
Quiero que todos los pacientes de herpes lean mi testimonio, mi nombre es SARAH MORGAN y soy de California en los EE. UU., Contraje herpes genital de mi ex novio que nunca tuvo ningún síntoma. Lo tengo desde hace 4 meses y ha afectado mi vida. Le he dicho a mis novios en quién confiaba y nunca he tenido una mala reacción, ha afectado mis nuevas relaciones con Smith y la gente piensa que el herpes es en realidad una irritación leve de la piel. El herpes tiene efectos a largo plazo sobre la salud. El estigma asociado a este virus por personas ignorantes es ridículo. La mayoría de las personas tienen herpes de una forma u otra. Me gustaría asesorar a la gente sobre cómo me deshago de mi herpes y estaba leyendo un comentario en Internet, y vi un testimonio publicado por una mujer de Alemania de que se deshizo de su herpes con la ayuda del Dr. AHKIGBE y así. Me alegré mucho cuando vi esa publicación, que su medicamento a base de hierbas es gratis y rápidamente recogí el correo electrónico del médico a base de hierbas y le envié un correo electrónico dentro de las 3 horas.Él respondió a mi correo electrónico y le explico cosas que me dijo que no me preocupara. me va a curar totalmente con su medicina herbal, solo pide un poco de dinero que usará para comprar los artículos para la preparación de la medicina herbal, ojalá se lo envíe porque el dolor era demasiado para mí y después de algunos días me dijo que había preparado la medicina a base de hierbas, que debería enviarle mi dirección que me la quiere enviar a través de DHL o FED-EX, así fue como obtuve la medicina a base de hierbas y la uso como me dijeron y Después de unos días descubrí que mi herpes ya no existía, fui al hospital para confirmar un Y realmente fue así como me curé. DR AKHIGBE también cura otras enfermedades mortales como, VIH / SIDA, HERPES, DIABETES, CÁNCER, ELA, ASMA, MENINGITIS, LUPUS, EPILEPSIA, ENFERMEDAD CRÓNICA, ENFERMEDAD DEL CORAZÓN., DOLOR DE ARTICULACIONES, DOLOR DE ESTÓMAGO, ESQUIZOFRENIA, POLIO, TUBERCULISPAS, ESCIZOFRENIA, POLIO, TUBERCULISPAS. ALZHEIMER, PARKINSON'S, para deshacerse amablemente a través de su correo electrónico: drrealakhigbe@gmail.com, comuníquese con su número: +2348025012866 sitio web: https://drrealakhigbe.weebly.com, aún puede escribirme en Instagram para obtener más información.
ResponderEliminar